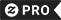Toque/clique na imagem para ver mais RealViewsTM
R$ 221,00
por cada gravata
Gravata Mesa periódica de IUPAC nova
Quantidade:
Sobre Gravatas
Feito por
Sobre Esse Design
Gravata Mesa periódica de IUPAC nova
A mesa do periodiс dos elementos químicos (também a mesa de Mendeleev, mesa periódica dos elementos ou apenas mesa periódica) é uma exposição tabular dos elementos químicos. Embora os precursores a esta mesa existam, sua invenção é creditada geralmente ao químico Dmitri Mendeleev do russo em 1869, que pretendeu a mesa ilustrar ("periódico") tendências de retorno nas propriedades dos elementos. A disposição da mesa foi refinada e estendido ao longo do tempo, enquanto os elementos novos foram descobertos, e os modelos teóricos novos foram desenvolvidos para explicar o comportamento químico. A mesa periódica é agora ubíquo dentro da disciplina académico da química, fornecendo uma estrutura extremamente útil para classificar, sistematizar, e comparar todos os muitos formulários diferentes do comportamento químico. A mesa encontrou a aplicação larga na química, na física, na biologia, e no planejamento, engenharia especialmente química. A mesa padrão atual contem 117 elementos em julho de 2009 em 1789, Antoine Lavoisier publicou uma lista de 33 elementos químicos. Embora Lavoisier agrupasse os elementos em gáss, em metais, em metalóides, e em terras, os químicos passaram o seguinte século que procurara por um esquema de classificação mais preciso. Em 1829, Johann Wolfgang Döbereiner observou que muitos dos elementos poderiam ser agrupados nas tríades (grupos de três) baseadas em suas propriedades químicas. O lítio, o sódio, e o potássio, por exemplo, foram agrupados junto como sendo metais macios, reactivos. Döbereiner igualmente observou que, quando arranjado pelo peso atômico, o segundo membro de cada tríade era aproximadamente a média do primeira e o terço. Isto tornou-se conhecido como a lei das tríades. [citação necessário] o químico alemão Leopold Gmelin trabalhou com este sistema, e em 1843 tinha identificado dez tríades, três grupos de quatro, e uns grupos de cinco. Jean Baptiste Dumas publicou o trabalho que descreve em 1857 relações entre vários grupos de metais. Embora os vários químicos pudessem identificar relações entre grupos pequenos de elementos, tiveram para construir ainda um esquema que os abrangeu todos. O químico alemão agosto Kekulé tinha observado em 1858 que o carbono tem uma tendência se ligar com outros elementos numa razão de um a quatro. O metano, por exemplo, tem um átomo de carbono e quatro átomos de hidrogênio. Este conceito tornou-se eventualmente conhecido como o valency. Em 1864, o químico alemão companheiro Julius Lothar Meyer publicou uma mesa dos 49 elementos conhecidos arranjados pelo valency. A mesa revelou que os elementos com propriedades similares compartilharam frequentemente do mesmo valency. O químico inglês John Newlands publicou uma série de papéis em 1864 e de 1865 que descreveram sua tentativa em classificar os elementos: Quando alistadas por ordem de aumentar o peso atômico, as propriedades físicas e químicas similares retornaram em intervalos de oito, que comparou às oitavas da música. Esta lei das oitavas, contudo, ridiculed por seus contemporâneos. [8] O retrato do professor Dmitri Ivanovich Mendeleev e Julius Lothar Meyer da química de Dmitri MendeleevRussian publicou independente suas mesas periódicas em 1869 e 1870, respectivamente. Ambos construíram suas mesas de forma semelhante: alistando os elementos em seguido ou a coluna por ordem do peso atômico e começando uma fileira ou uma coluna nova quando as características dos elementos começaram a repetir. O sucesso da mesa de Mendeleev veio de duas decisões que fez: O primeiro era deixar diferenças na mesa quando pareceu que o elemento correspondente não tinha sido descoberto ainda. Mendeleev não era o primeiro químico a fazer assim, mas foi uma etapa mais usando as tendências em sua mesa periódica prever as propriedades daqueles elementos faltantes, tais como o gálio e o germânio. A segunda decisão era ignorar a ordem sugerida pelos pesos atômicos e comutar ocasionalmente elementos adjacentes, tais como o cobalto e o níquel, para classificá-los melhor em famílias químicas. Com o desenvolvimento das teorias da estrutura atômica, tornou-se aparente que Mendeleev tinha alistado inadvertidamente os elementos por ordem de aumentar o número atômico. Com o desenvolvimento de teorias mecânicas do quantum moderno de configurações do elétron dentro dos átomos, tornou-se aparente que cada fileira (ou o período) na mesa corresponderam ao enchimento de um escudo do quantum dos elétrons. Na mesa original de Mendeleev, cada período estava ao mesmo comprimento. Contudo, porque os átomos maiores têm mais secundário-escudos do elétron, as mesas modernas têm uma pena mais adicional de uns períodos progressivamente mais longos a mesa. Nos anos que seguiu depois que Mendeleev publicou sua mesa periódica, as diferenças que deixou foram enchidas enquanto os químicos descobriram uns elementos mais químicos. O último elemento natural a ser descoberto era Francium (referido por Mendeleev como o eka-césio) em 1939. A mesa periódica igualmente cresceu com a adição de elementos sintéticos e transuranic. O primeiro elemento transuranic a ser descoberto era o neptúnio, que foi formado bombardeando o urânio com nêutrons em uma mesa periódica de elementos periódica do ciclotrão em 1939 "mesa" do actínio orbital radioativo atômico molecular biológico bioquímico analítico físico orgânico do período da fileira do quantum da rotação do núcleo de Molarity do isómero do isótopo do trítio do deutério do elétron do nêutron de Proton do peso atômico" do átomo do símbolo químico" do símbolo "da fórmula "de Avogadro da toupeira da molécula dos compostos do composto do biólogo da biologia da bioquímica do bioquímico de agosto Kekulé do poster da carta das experiências da experiência do laboratório do laboratório de física da química dos produtos químicos do químico de Dmitri Mendeleev Antoine Lavoisier dos elementos do érbio de alumínio do einsteinio do Dysprosium de Darmstadtium Dubnium do cúrio do cobre do cobalto do cromo do cloro do césio do cério do carbono do califórnio do cálcio do cádmio do bromo do boro de Bohrium do bismuto do berílio do berquélio do bário do Astatine do arsênico do argônio do antimónio do amerício Do neodímio Dourado do molibdênio de Mercury do mendelévio de Meitnerium do manganês do magnésio do Lutetium do lítio da ligação do Lawrencium do crípton do ferro do irídio do iodo do índio do hidrogênio do Holmium do hélio de Hassium do háfnio do germânio do gálio do gadolínio do Francium do flúor do férmio do európio zircónio de urânio de néon do zinco do ítrio do Ytterbium do xénon do vanádio de Ununbium Ununnilium Ununumium do tungstênio de TinTitanium do Thulium do tório do tálio do Terbium do telúrio do Tc do tântalo do enxofre do estrôncio do sódio da prata do silicone do selênio de Seaborgium do escândio do Samarium do Rutherfordium do ruténio do rubídio do ródio do rénio do rádon do rádio do Protactinium do Promethium do Praseodymium do potássio do polónio do plutônio da platina do fósforo do paládio do oxigênio do ósmio do nobélio do nitrogênio do nióbio do níquel do neptúnio
Tradução Automática
Comentários de clientes
4.3 de 5 estrelas20 Total de Comentários
20 Avaliações
Avaliações de produtos similares
5.0 de 5 estrelas
5 de 5 estrelasPor 18 de outubro de 2022 • Compra segura
Gravata
Programa de revisão da Zazzle
Excelente produto e qualidade. Perfeito sem falhas
5.0 de 5 estrelas
5 de 5 estrelasPor 9 de dezembro de 2011 • Compra segura
Gravata
Programa de revisão da Zazzle
Era o que eu esperava. Estou SATISFEITO.
Destaco a atenção que a mim foi dispensada pelo SAC através da Srª PATRÍCIA.
MUITO EDUCADA E ATENCIOSA. MUITO BOA.
5.0 de 5 estrelas
5 de 5 estrelasPor 13 de maio de 2014 • Compra segura
Gravata
Programa de revisão da Zazzle
muito bom material de bom gosto. é bem delicado e discreto
Tags
Outras Informações
Identificação do Produto (ID): 151732490403501565
Criado em: 29/10/2011 6:52
Avaliação: G