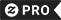Toque/clique na imagem para ver mais RealViewsTM
R$ 60,75
por cada chaveiro
Chaveiro Radon Elemento Individual da Mesa Periódica
Quantidade:
Modelo
Círculo de Alumínio
+R$ 15,90
+R$ 15,90
+R$ 78,25
+R$ 78,25
Sobre Porta chaves
Feito por
Sobre Esse Design
Chaveiro Radon Elemento Individual da Mesa Periódica
A mesa periodiс dos elementos químicos (também a mesa de Mendeleev, a mesa periódica dos elementos ou apenas a mesa periódica) é uma exibição tabular dos elementos químicos. Embora existam precursores dessa mesa, sua invenção é geralmente creditada ao químico russo Dmitri Mendeleev em 1869, que pretendia que a mesa ilustrasse tendências recorrentes ("periódicas") nas propriedades dos elementos. A disposição da mesa foi refinada e ampliada com o tempo, à medida que novos elementos foram descobertos, e novos modelos teóricos foram desenvolvidos para explicar o comportamento químico. A mesa periódica já é onipresente na disciplina acadêmica da química, fornecendo um quadro extremamente útil para classificar, sistematizar e comparar todas as diferentes formas de comportamento químico. A mesa encontrou ampla aplicação em química, física, biologia e engenharia, especialmente em engenharia química. A atual mesa-padrão contém 117 elementos a partir de julho de 2009 Em 1789, Antoine Lavoisier publicou uma lista de 33 elementos químicos. Embora Lavoisier tenha agrupado os elementos em gases, metais, não metais e terras, os químicos passaram o século seguinte buscando um esquema de classificação mais preciso. Em 1829, Johann Wolfgang Döbereiner observou que muitos dos elementos poderiam ser agrupados em tríades (grupos de três) com base em suas propriedades químicas. O lítio, o sódio e o potássio, por exemplo, foram agrupados como metais leves e reativos. Döbereiner também observou que, quando arranjado por peso atômico, o segundo membro de cada tríade era aproximadamente a média do primeiro e do terceiro. Isso ficou conhecido como Lei de Tríades. O químico alemão Leopold Gmelin trabalhou com esse sistema e, em 1843, identificou dez tríades, três grupos de quatro e um grupo de cinco. Jean Baptiste Dumas publicou trabalhos em 1857 descrevendo relações entre vários grupos de metais. Embora vários químicos tenham conseguido identificar relações entre pequenos grupos de elementos, eles ainda tinham de construir um esquema que os abarcasse a todos. O químico alemão August Kekulé havia observado em 1858 que o carbono tem tendência a se ligar a outros elementos numa proporção de um a quatro. O metano, por exemplo, tem um átomo de carbono e quatro átomos de hidrogênio. Este conceito acabou por se tornar conhecido como valência. Em 1864, o colega químico alemão Julius Lothar Meyer publicou uma mesa dos 49 elementos conhecidos arranjados por valência. A mesa revelou que elementos com propriedades semelhantes muitas vezes compartilhavam o mesmo valor. O químico inglês John Newlands publicou uma série de artigos em 1864 e 1865 que descreviam sua tentativa de classificar os elementos: Quando listado por ordem de aumento do peso atômico, retomavam-se propriedades físicas e químicas similares em intervalos de oito, que ele comparava com as oitavas da música. Esta lei das oitavas, porém, foi ridicularizada pelos seus contemporâneos[8]. Retrato de Dmitri MendeleevO professor de química russo Dmitri Ivanovich Mendeleev e Julius Lothar Meyer publicaram independentemente suas mesas periódicas em 1869 e 1870, respectivamente. Ambos construíram suas mesas de forma semelhante: ao listar os elementos em uma linha ou coluna em ordem de peso atômico e iniciar uma nova linha ou coluna quando as características dos elementos começaram a se repetir. O sucesso da mesa de Mendeleev veio de duas decisões que ele tomou: a primeira foi deixar lacunas na mesa quando parecia que o elemento correspondente ainda não havia sido descoberto. Mendeleev não foi o primeiro químico a fazê-lo, mas foi um passo adiante usando as tendências de sua mesa periódica para prever as propriedades desses elementos faltando, como gálio e germânio. A segunda decisão foi ignorar ocasionalmente a ordem sugerida pelos pesos atômicos e trocar elementos adjacentes, como cobalto e níquel, para melhor classificá-los em famílias químicas. Com o desenvolvimento de teorias da estrutura atômica, ficou claro que Mendeleev havia listado inadvertidamente os elementos para aumentar o número atômico. Com o desenvolvimento de teorias mecânicas quânticas modernas de configurações de elétrons dentro dos átomos, tornou-se evidente que cada fileira (ou período) na mesa correspondia ao preenchimento de uma casca quântica de elétrons. Na mesa original de Mendeleev, cada período tinha o mesmo comprimento. Mas, como átomos maiores têm mais sub-cascas de elétrons, as mesas modernas têm progressivamente períodos mais longos na mesa. Nos anos seguintes a Mendeleev publicou sua mesa periódica, as lacunas que deixou foram preenchidas à medida que os químicos descobriam mais elementos químicos. O último elemento natural a ser descoberto foi Francium (referido por Mendeleev como eka-césio) em 1939. A mesa periódica também cresceu com a adição de elementos sintéticos e transurânicos. O primeiro elemento transurânico a ser descoberto foi o neptunium, formado pelo bombardeio de urânio com nêutrons em um cíclotron em 1939 "Mesa periódica de elementos" Mesa periódica de elementos Dmitri Mendeleev Antoine Lavoisier Química Física Laboratório de Física de Química Laboratório Gráfico Poster de agosto Kekulé Biológico Bioquímico Bioquímica Biologia Biológica Compostos Moléculas Moléculas Mole Avogadro Símbolo Químico Atom Atômica "Peso Atômico" Proton Neutron Elétron Deuterium Tritium Isomer Molaridade Núcleo Radioativo Spin Orbital Quantum Período de Fila Actínio Alumínio Amerício Antimonia Argon Arsenic Astatine Barium Berkelium Beryllium Bismuth Bohrium Boron Bromine Cadium Calcium califórnium Cério Cério Cério Cromo Cobalto Cúrilo Darmstadtium Dubnium Dysprosium Einsteinium Erbium Ferium Fluorine Francium Gadolínio Gallium Germanium Dourado Háfnio Hélio Holium Indio Iodina Irídio Ferro Krypton Lítio Lítio Lítio Lécio Magnésio Manganês Mântalio Manalédico Molibdênio Neodímio Níon Nítio Níbio Níóbio Níóbio Níódulo Níon Ósmio Palládio Fósforo Pósforo Putônio Polônio Potássio Prometio Protactinium Radium Radon Rhenium Rubidium Ruthenium Rutherfordium Samarium Scandium Seaborgium Selenium Silício Sódio Sódio Estrôncio Sódio Sódio Sódio Túncio Tântalo Tântalo Tântalo Télio Télio TinTitânio Tungstênio Ununbio Urânio Ununununununum Urânio Vênio Xênon Térbio Ítrio Zircônio Zinco
Tradução Automática
Comentários de clientes
4.8 de 5 estrelas24 Total de Comentários
24 Avaliações
Avaliações de produtos similares
5 de 5 estrelas
Por 3 de janeiro de 2023 • Compra segura
Programa de revisão da Zazzle
Material de excelente qualidade e impressão em alta resolução. Excelente qualidade de impressão
Produto original
5 de 5 estrelas
Por 29 de abril de 2019 • Compra segura
Chaveiro Círculo de Metal, 5,08cm
Programa de revisão da Zazzle
Escolhi um chaveiro que faz alusão ao apelido do presenteado. Muito difícil encontrar presentes originais. É só um chaveiro simples; é barato, mas bonito. O importante era poder dar o recado, e o produto é bom e é atraente. O problema é que, por ser importado, custou imposto e embalagens bem acima do próprio produto. Sim, o produto é perfeito. Muito bonito.
5 de 5 estrelas
Por 14 de junho de 2013 • Compra segura
Chaveiro Círculo de Metal, 5,08cm
Revisão do Criador
Excelente compra, tudo certinho!... Recebi a mercadoria embalada de forma que não estragasse o produto!... Muito bom! Impressão perfeita, cores exatas com a imagem original, acabamento sensacional!.. tudo muito bem feito!... Gostei muito!
Tags
Outras Informações
Identificação do Produto (ID): 146093409345160759
Criado em: 15/01/2013 7:41
Avaliação: G
Itens visualizados recentemente